Abiomed:全球最小心脏泵Impella ECP不确定的商业化之路
长期以来,终末期心衰患者缺乏有效的治疗手段,已有药物和心率控制器械难以逆转病程进展,心脏移植因受限于供体来源,无法惠及大众,经导管心脏泵(VAD)成为广大终末期心衰患者有效地延长生命、提高生活质量的唯一希望。
近10余年来,VAD技术发展取得了突破,其在发达国家的临床应用进展迅速,已发展成终末期心衰的标准治疗手段。Abiomed(阿比奥梅德)公司成立于1981年,在全球VAD领域有领先地位,公司生产的Impella心脏泵,是唯一获得美国 FDA 批准适用于需要高危PCI(经皮冠状动脉介入治疗)或心源性休克等严重冠状动脉疾病患者的经皮心脏泵技术。目前,全球使用Impella心脏泵的患者超过21万。
2004年以来, Abiomed成为增长最快美股医疗器械公司,过去10年中Abiomed在标普 500 指数中的所有股票中表现位居前三,公司市值近150亿美元。回顾Abiomed的发展历史,或对国内同类型创业公司有借鉴之意。
手握核心产品,不断投资并购
1981年,Abiomed开始人工心脏的开发。创始人Lederman与德克萨斯心脏研究所合作开发了植入式全人工心脏AbioCor。在2001年至2004年的临床试验期间,仅有14台AbioCor设备被植入人体,其中寿命最长的接受者存活了512天。2006年AbioCor获得 FDA 批准,适用于濒死且不符合心脏移植资格的患者。
2005年,Abiomed收购德国亚琛的心室辅助设备公司Impella CardioSystemsAG,此后公司的发展重心便逐渐转向心肺康复领域,并不断在介入泵小型化的技术创新与急症生命支持进行全场景布局,布局了Impella系列产品。
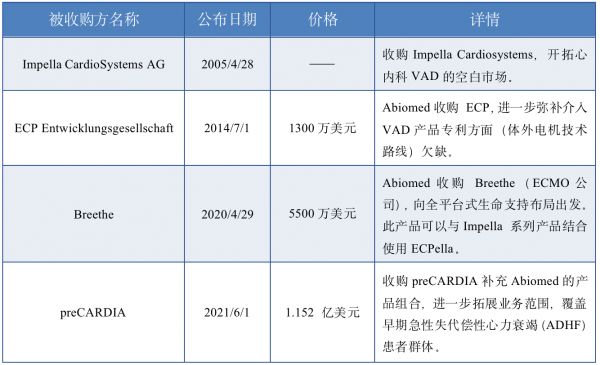
Abiomed收购情况表
通过上述收购和自研,目前,Abiomed公司产品线包括 Impella产品组合、Abiomed Breethe OXY-1 System™心肺支持系统(ECMO)& ECPella和preCARDIA,覆盖的临床适应症主要包含:高危PCI、心源性休克、右心衰竭及严重肺衰竭。
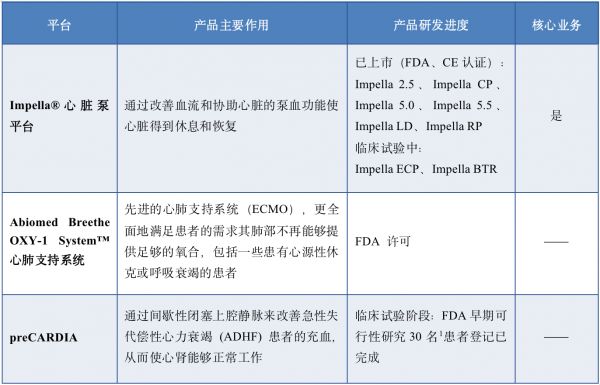
Abiomed产品线布局、作用及产品研发进度
而作为目前全球唯一获得FDA认证的介入式人工心脏,Impella系列产品在全球介入心脏泵领域罕有对手。2021财年Impella系列产品销售额达到8.06亿美元,收入占公司总营收超95%,为Abiomed公司绝对核心业务。
其中,Impella CP的销售收入占比为77%,是Impella系列中销售收入占比最高的产品。由此可见在介入式心脏泵为患者提供循环支持当前的临床需求中,相较于大流量和小流量产品,中流量产品临床应用范围更广。
当前Impella系列共计6款产品上市,2款正处于临床阶段,通过布局不同流量,左右心室,实现临床不同需求点覆盖。通过其产品线布局,可以看出Impella产品未来将朝着更小尺寸、更长使用时间、更大流量方向、智能化方向发展。
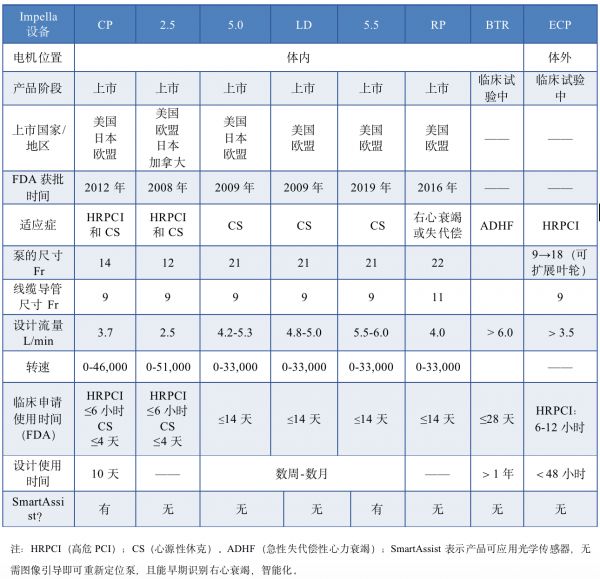
Impella系列产品参数对比
其中值得关注的是Impella ECP,它是Abiomed于2014年收购位于德国柏林的医疗器械公司ECP后开始研发的一款世界上最小的血流动力学支持型心脏泵。与以往Impella系列产品所采用的体内电机驱动技术不同的是,Impella ECP延续了ECP公司正在研发的体外电机驱动技术,即通过外部驱动轴增加心脏的血液循环。
作为全世界最小的人工心脏,Impella ECP所使用的护套和泵仅9 Fr(约3 mm),在降主动脉中卸下护套,心脏泵(叶轮)可扩展到约18 Fr,手术完成后,心脏泵缩小并重新套回至9 Fr护套,其峰值流量大于每分钟3.5 L。
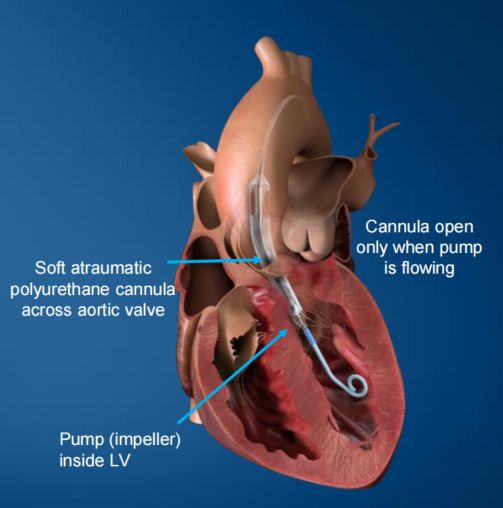
图3 Impella ECP产品
2020年6月,FDA批准Abiomed研究用Impella ECP心脏泵医疗器械豁免(IDE)申请,即将进行首次人体试验以验证其早期可行性;10月,首批患者(2人)接受Impella ECP治疗。2021年8月,FDA授予Impella ECP可扩展经皮心脏泵突破性设备名称(早期可行性研究已完成21名患者的治疗)。根据Abiomed提交的“Impella ECP 早期可行性研究”临床试验方案,临床试验预计主要完成日期为2022年2月,但截至2022年5月,项目仍处于志愿者招募状态。
八年之久,Impella ECP上市时间仍未可知,“难产”的Impella ECP到底难在吗?难以攻克的电机驱动可靠性技术难题和使用安全性或许是主要原因。
从“体外”到“体内”
目前介入式人工心脏从技术路线上来看,主要分为2种:体内电机技术和体外电机技术。两种技术路线于20世纪90年代同步开始研究。
全球范围内,当前拥有体内电机式介入泵相关技术专利的企业仅有Abiomed一家;体外电机技术专利企业目前仅4家,能查到公司经营信息的仅3家,分别为Abiomed、MAGENTA MEDICAL LTD.(Abiomed投资)和雅培(介入产品)。
Abiomed体内电机技术来源于2005年收购的Impella CardioSystems AG公司,2008年首款获得FDA许可的Impella 2.5至今仍在使用。目前,Abiomed公司应用体内电机技术已开发出多款涵盖不同流量/功能组合的产品。体内电机技术路线由于其微型化体内电机技术的高难度、高壁垒,目前全球仍无除Abiomed外其它公司可以突破。
在体外电机路线下,唯一一款上市产品雅培HeartMate PHP已于2021年退市,Abiomed应用体外电机技术所研发的Impella ECP临床试验进度过缓,至今仍未上市。
这就表示,体外电机技术路线下,截至目前还无一款成熟的商业化产品,体外电机介入心脏泵的安全性、可靠性仍无法得到较好的临床验证、领域专家认可。究其原因,从机械结构上来看,体外电机的柔性轴传动不可避免会带来可靠性差,停泵风险高的潜在隐患,而这亦是雅培HeartMate PHP退市的主要原因。
雅培HeartMate PHP由曾经的专注心室辅助设备的Thoratec公司开发。2015年,圣犹达医疗公司收购Thoratec公司,2016年4月,雅培收购圣犹达医疗公司(包含Thoratec),最终HeartMate PHP产品归属雅培旗下。2017年,雅培因电机停止运行的设备故障,宣布暂停其HeartMate PHP SHIELD II研究的注册并停止在欧洲的商业销售。2021年,雅培中止HeartMate PHP SHIELD II的试验注册,中止原因是由于程序结束时叶轮速度降低,产品无法满足其预期服务的患者的需求。
也因此,我们预测,即便最终Impella ECP顺利上市,由于其临床设计术中使用时间为48小时(申请临床试验术中使用时间:6-12小时),而Impella CP临床设计术中支持时间为10天(申请临床试验术中使用时间:FDA-4天,CE-5天),因此Impella ECP临床应用场景将局限于高危PCI术中短期循环支持,无法进一步拓展适应症至长时间需求的心源性休克,Impella ECP在覆盖人群及商业化上,可能只是作为Impella CP的一个补充,市场空间有限。

体内电机技术和体外电机技术对比
综合来看, 体内电机技术路线仍将是最有效、安全可靠的技术能够进行临床应用,未来介入心脏泵市场仍将占全球心血管介入泵市场的绝对主导份额。从Abiomed公司未来发展规划来看,当前及未来的核心重点资源仍将持续投放在以体内电机技术为基础的Impella系列产品的优化改进、临床适应症拓展及海外潜在市场拓展上,还有长足发展空间。相关推荐
“心擎医疗”完成5亿元C轮融资,开启中国体外磁悬浮人工心脏新时代丨钛快讯
36氪首发 | 心衰赛道企业「心擎医疗」完成近5亿元C轮融资,红杉中国领投
全球第一个 3D 打印的「人造心脏」诞生了
或设计制造医疗器械装置,「清科博动」拥有多项心脏泵专利
36氪首发 | 让危重病人重获“心”生,人工心脏研发公司「心擎医疗」获得超亿元B轮融资
比芝麻还小的心脏每分钟跳动60到100次,《细胞》重磅:「mini 心脏」培育成功
替代心脏移植,人工心脏研发企业「同心医疗」获蓝帆医疗1亿元投资
这条哈佛用心脏细胞做出的“人造鱼”,游了108天,登上Science
36氪首发 | 研发超小型磁悬浮人工心脏,「核心医疗」获数千万元天使轮融资
千亿美金的中国心脏
网址: Abiomed:全球最小心脏泵Impella ECP不确定的商业化之路 http://m.xishuta.com/zhidaoview25488.html
